양자화 된 에너지의 대해 학습하는 내용이다. 물리 또는 물리화학과 연결이 되어 있지만, (물론, 양자화학과도 밀접한 관련이 있다.) 지금 간단한 내용 등을 숙지하면 좋을 것으로 본다. 고등학교 화학시간에 배운 오비탈 관련 내용이 언급되는데, 그렇게 어려운 부분은 아닐 것을 생각된다. 화학 시험에 자주 나오는 내용도 포함하니, 기본부터 다지는 생각으로 했음 좋겠다.
Chapter 6. 원자의 전자 구조 (Electronic Structure of Atoms)
1. 전자기 복사와 양자화된 에너지
- 빛과 같은 전자기파는 "파장 (λ)"과 "진동수 (ν)"를 가지며, 빛의 속도는 c = λ ν
- 플랑크 (Planck)의 양자 이론: 에너지는 연속적이지 않고 특정 값(양자)으로만 존재.
- 광전 효과 (Photoelectric Effect): 아인슈타인은 빛을 입자(광자, photon)로 설명.
- 광자의 에너지: E=hν, h=6.626×10−34J⋅s (플랑크 상수)


2. 수소 원자의 선 스펙트럼과 보어 모형
- 수소 원자는 특정 파장(선 스펙트럼)만 방출 → 전자가 특정 에너지 준위에서만 존재함을 의미.
- 보어의 원자 모형: 전자는 특정 궤도에 있으며, 높은 궤도에서 낮은 궤도로 이동 시 빛 방출.

3. 물질파와 불확정성 원리
- 드브로이 (de Broglie): 전자는 입자이면서 파동의 성질도 가짐 (λ=h/mv).
- 하이젠베르크 (Heisenberg)의 불확정성 원리: 전자의 위치와 운동량을 동시에 정확히 측정할 수 없음.
4. 양자역학과 오비탈 (Orbital)
슈뢰딩거 방정식 → 전자는"오비탈(전자 밀도가 높은 공간)"에 존재.
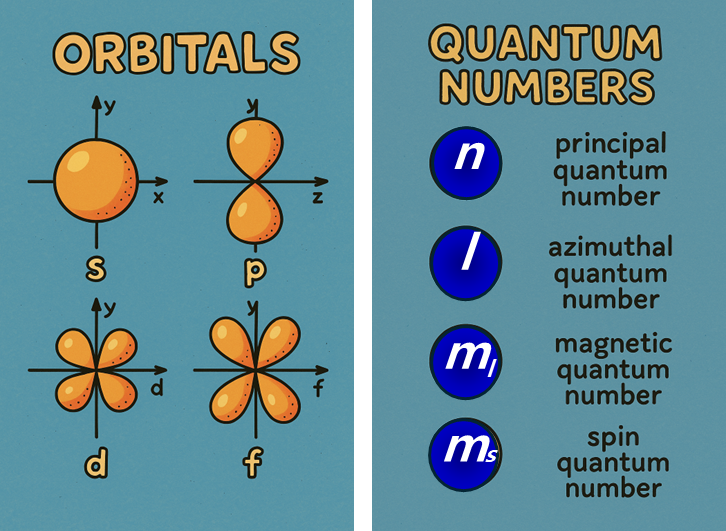
오비탈의 종류:
주양자수 (n): 에너지 수준 (1, 2, 3, ...)
부양자수 (l): 오비탈 형태 (s,p,d,f)
자기양자수 (ml): 오비탈 방향
스핀양자수 (ms): 전자 스핀 (+1/2,−1/2)
5. 다전자 원자의 전자배열과 주기율표
- 파울리 배타 원리: 한 오비탈에 최대 2개의 전자, 스핀은 반대 방향.
- 훈트 규칙: 동일한 에너지를 가지는 오비탈에는 전자가 한 개씩 채워진 후 짝을 이룸.
- 전자배열: 원소의 전자는 에너지 준위가 낮은 오비탈부터 채워짐
예: 탄소 (C): 1s2 2s2 2p2 / 플루오린 (F): 1s2 2s2 2p5
6. 주기율표와 원소의 종류
- 주족 원소: s,p 궤도 전자 배치를 따름 (알칼리 금속, 할로젠 등)
- 전이 금속: d 궤도 전자를 가짐
- 란타넘족 및 악티늄족: f 궤도 전자를 가짐
- 원소의 주기율표 위치를 통해 전자배열과 성질 예측 가능.
많은 이야기 들이 있지만, 각 이야기 (주제)들은 화학에서 중요한 부분을 차지한다. 파울리배타원리라든가 훈트규칙 관련해서는 시험문제로도 많이 나오는 부분이라 할 수 있겠다. 전자 배열이 어떻해 이루어지는지를 확인하는 것 역시 빼 놓을 수 없는 부분이다. 쉽게 설명할려고 하고 있으니, 약간의 시간을 내서 읽어보았음 한다.
'일반화학' 카테고리의 다른 글
| Chapter 7_Intro_원소의 주기적 성질 (0) | 2025.04.10 |
|---|---|
| Chapter 6_Zeeman Effect (0) | 2025.04.09 |
| 쉬어가기_이온이란 무엇인가? (0) | 2025.04.06 |
| 쉬어가기_플랑크의 양자이론 (Planck’s Quantum Theory) (0) | 2025.04.05 |
| Chapter 5-B_열화학 (0) | 2025.04.04 |